
该药品基于药品上市许可持有人制度(MAH),在闵行研发申报、在临港新片区受托生产。武田中国负责该产品在中国内地、中国香港和中国澳门的商业化进程。双方将整合各自资源优势,加速为患者提供突破性的基因疗法。
该药品自2021年进入临床试验至获批上市期间,国家药监局药品审评核查长三角分中心与上海市药监局组建专门服务团队,在检验、审评、核查、生产许可等注册上市的全环节持续跟踪辅导,并联合市科委、闵行区政府、临港管委会等部门多措并举、精准发力,共同支持企业创新研发,让企业少走“弯路”,加快注册上市进程。
对于大家最关心的价格问题——目前,全球已有3款用于血友病的基因治疗产品上市,分别为BioMarin的Roctavian(2023.6 FDA)、CLS/uniQure的Hemgenix(2022.11 FDA)、辉瑞的Beqvez(2024.4 FDA),分别用于治疗A型血友病、B型血友病、B型血友病。
定价方面,Roctavian、Hemgenix、Beqvez分别定价290万美元、350万美元、350万美元。但是商业化却远不及预期。据公开报道,来自BioMarin的年报显示,2023年仅3名患者接受Roctavian治疗,销售为350万美元。
目前,这款基因治疗药物的定价还未公布,但可以肯定的是,对比国外同类,会低很多。
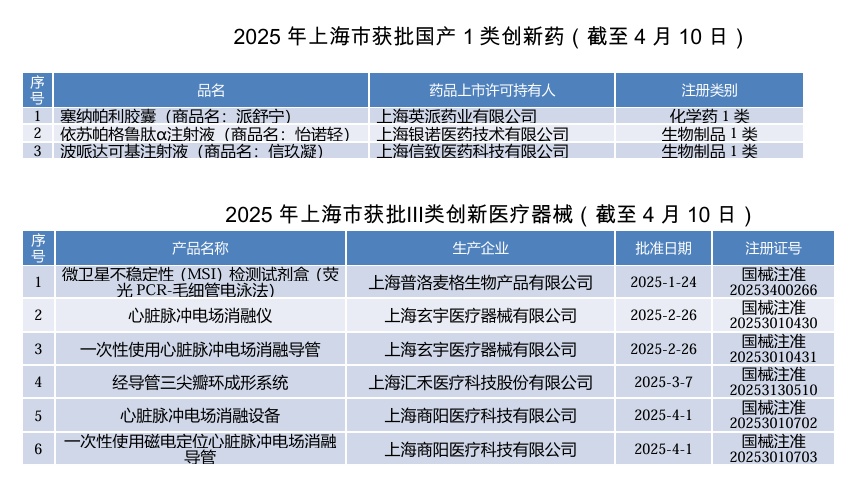
今年以来,上海共有3款国产1类创新药、6款Ⅲ类创新医疗器械获批上市。市药监部门正深入实施“一清单、两优化、三联动”服务创新机制,针对重点产品和重点项目实施“提前介入、专人专班、一企一策、全程指导”,助力创新产品研发上市;加强产品上市后监管,保护患者用药用械安全。
转载请注明来自今日闵行官方微信