编译:高杰
当人类被细菌、真菌等病原体侵袭时,抗生素往往是临床治疗的“主力军”。但随着耐药性问题日益严峻——全球每年因耐药菌感染死亡的人数已超百万,传统抗感染药物的效果不断打折扣,寻找全新的抗感染策略迫在眉睫。
9月2日,国际知名期刊《细胞·生物材料》发表的一项研究取得突破性进展:宾夕法尼亚大学和杜克大学的研究人员成功利用生成式人工智能技术创造出多种高效抗菌肽,为解决抗生素耐药性问题带来了新希望。实验数据显示,这些AI设计的抗菌肽对多种超级耐药菌表现出极强的杀灭能力。

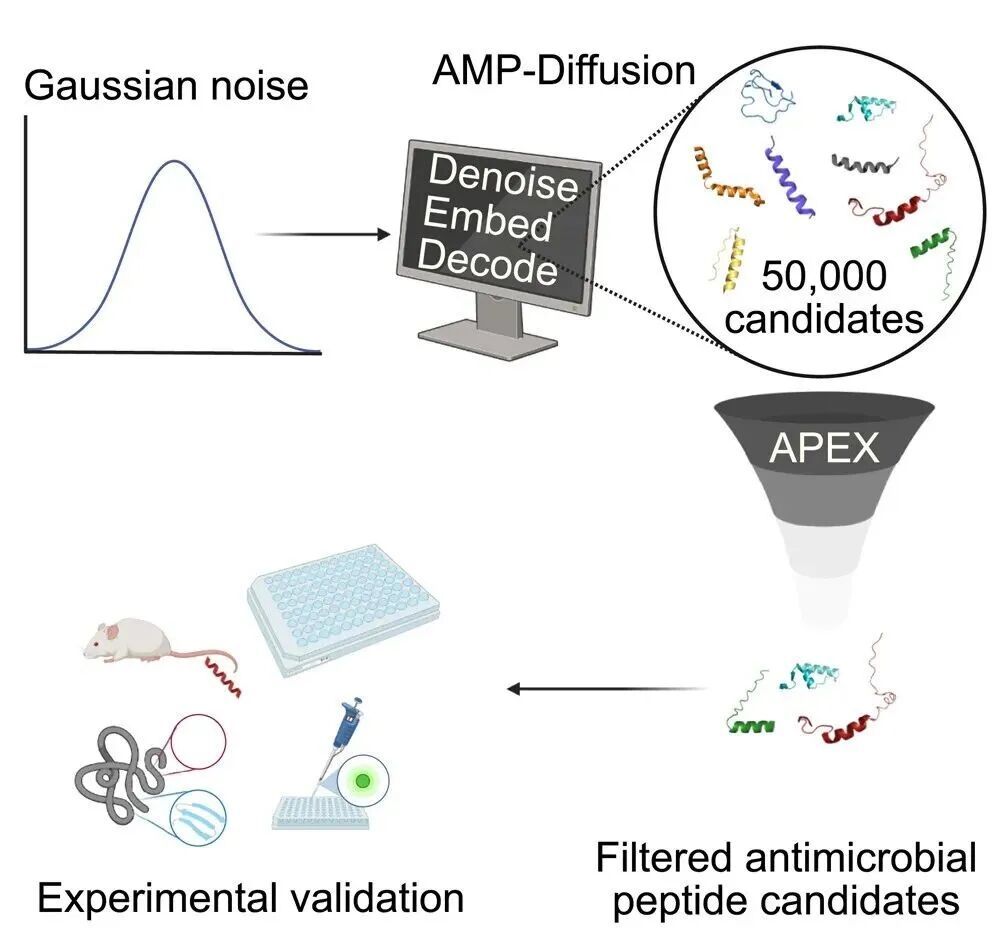
抗生素的发现曾是医学史上最伟大的成就之一。然而,过度使用和滥用导致细菌产生耐药性,使许多传统抗生素逐渐失去效果。世卫组织已将抗生素耐药性列为全球十大公共卫生威胁之一。
更令人担忧的是,新抗生素的研发速度远远跟不上细菌产生耐药性的速度。研发一种新抗生素通常需要10年以上时间,投入资金超过10亿美元,而细菌产生耐药性可能只需要2-3年。
抗菌肽是生物体内天然存在的短链氨基酸,是先天免疫系统的重要组成部分。从人类到植物,几乎所有生物都依靠抗菌肽来抵御病原体入侵。
与传统抗生素不同,抗菌肽通过物理机制破坏细菌细胞膜,导致细胞内容物外泄而死亡。这种作用机制使得细菌很难产生耐药性。
然而,天然抗菌肽存在稳定性差、毒性较大等问题。科学家们一直试图通过修饰天然抗菌肽来优化性能,但进展缓慢。传统的试错方法需要合成和测试大量候选分子,效率极低。
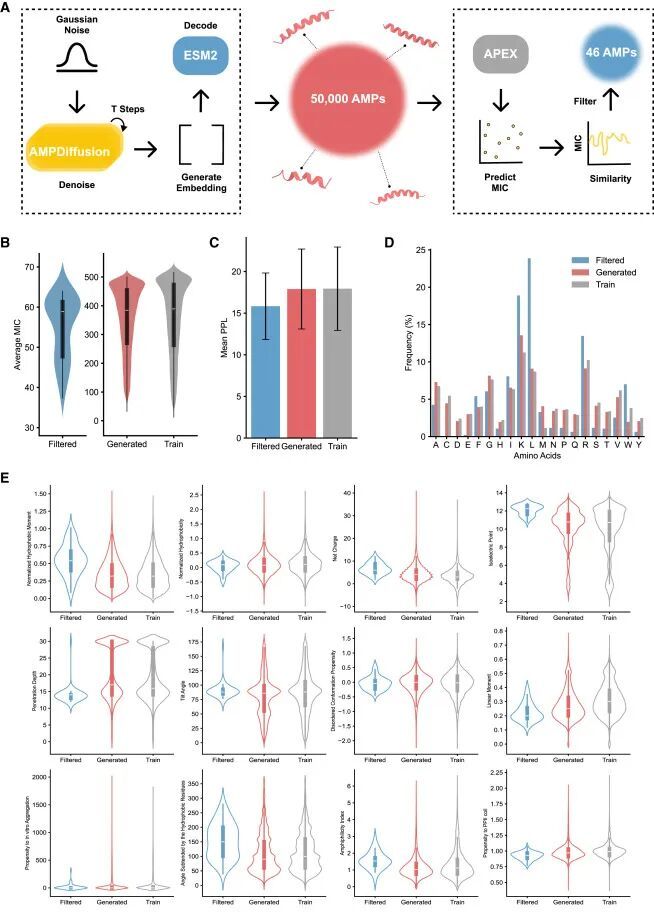
AMP-Diffusion模型和生成肽的特性
这项新研究采用了“生成式潜在扩散语言模型”的人工智能技术,彻底改变了抗菌肽的设计方法。
研究团队首先训练AI系统学习了已知抗菌肽序列的“语言规则”,就像理解人类语言一样理解蛋白质的“氨基酸语言”,最终自主生成全新的、自然界中不存在的抗感染序列,整个过程实现了“从模仿到创造”的跨越。
该模型的优势在于它不仅模仿现有抗菌肽,而是真正理解了氨基酸序列与抗菌功能之间的关系,从而能够进行自主创造。
研究团队使用AMP-Diffusion生成50000个候选抗菌肽序列,并用APEX深度学习模型对其进行筛选,最终合成并实验测试了46个抗菌肽序列,结果令人振奋:
▲这些AI设计的抗菌肽对耐甲氧西林金黄色葡萄球菌(MRSA)、耐碳青霉烯类肺炎克雷伯菌(CRKP)等多种超级耐药菌表现出极强的杀灭能力。
▲某些AI设计的抗菌肽效果甚至超过了临床常用的传统抗生素。实验数据显示,这些新型抗菌肽能够在很低的浓度下就有效抑制细菌生长。
▲更重要的是,这些抗菌肽同时保持了较高的安全性,对人类细胞显示出低毒性,具有很好的选择性毒性——能够杀死细菌却不伤害人体细胞。
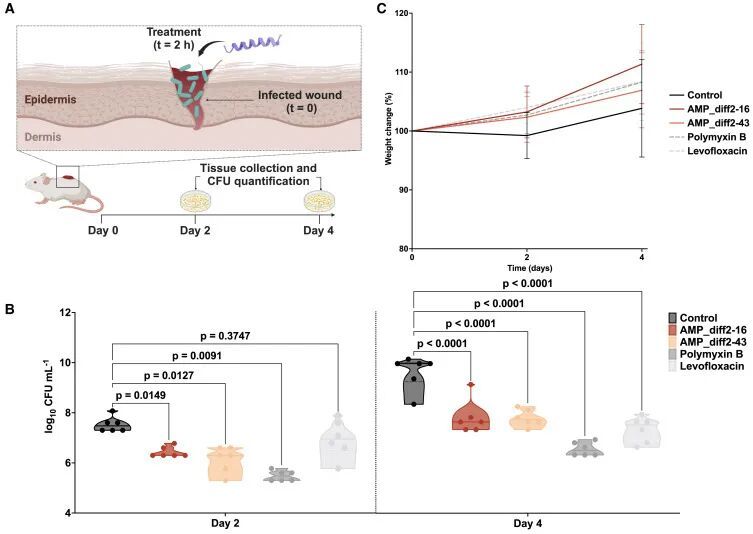
小鼠感染模型中肽的抗感染活性
进一步机制研究表明,这些AI设计的抗菌肽一部分亲水,一部分疏水,这种结构使它们能够与细菌细胞膜结合并形成孔洞,导致细胞内容物外泄。由于细菌细胞膜与人类细胞膜在成分和结构上存在差异,这些抗菌肽能够选择性攻击细菌细胞,而不伤害人类细胞。
AI设计的创新性在于,它能够探索人类研究者可能忽略的氨基酸组合,发现意想不到的有效序列。这些序列在自然界中可能不存在,但却具有理想的抗菌特性。
这项研究的意义远不止于抗菌肽设计本身,它展示了人工智能在生物医学领域的巨大潜力,特别是在药物研发方面。
研究人员表示,同样的方法可以应用于其他治疗性肽类的设计,如抗癌肽、抗病毒肽、抗炎肽等。AI甚至可以为特定患者群体量身定制个性化治疗方案。
数据图及从参考来源:
https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(25)00174-6